5 КВІТНЯ 2016 РОКУ.
ВІДКРИТИЙ УРОК
З ХІМІЇ
У
7-В КЛАСІ
ВЧИТЕЛЯ БІОЛОГІЇ ТА ХІМІЇ
ПЛЯСЕЦЬКОЇ ЯНИ СЕРГІЇВНИ.
УРОК № 42.
Кількісний склад розчину. Масова
частка розчиненої речовини.
Мета: ознайомити учнів із
сособами вираження складу розчинів, поняттями «масова частка розчиненої
речовини», «концентрація». Формувати
навички використання цих понять для обчислення й приготування розчинів.
Обладнання: підручник
«Хімія. 7 кл.» , тестові завдання на
картках, картки з умовами задач, терези,
важки, колба, мірний циліндр, стакан з водою, сіль.
Тип уроку: формування нових
знань, умінь, навичок.
Хід
уроку
І. Актуалізація опорних знань.
Бесіда
Дайте відповіді на
запитання: «Яке, на вашу думку, значення мають розчини у житті та практичній
діяльності людини?» (Заслуховуються
відповіді учнів. Технологія «мікрофон».)
Розчини
мають величезне значення в органічному й неорганічному (мінеральному) житті
Землі, а також у науці й техніці. Сьогодні на уроці ми розглянемо такі питання:
1. Що таке розчин?
2. Яка відмінність між розчинами й механічними сумішами?
3. Як класифікують розчини?
4. Чим відрізняються істинні розчини від зависей?
Експрес-тести з теми «Розчини»
(7-10 хв)
Варіант І
1.
Виберіть,
у яких випадках утворяться істинні розчини, якщо речовини добре перемішати у
воді:
А.Глина; Б. Спирт; В. Олія; Г. Цукор.
2. Компонент розчину, який перебуває у тому самому
агрегатному стані, що й розчин, називається:
А.Розчинена
речовина; Б. Розчинник; В. Розчин.
3. Використовуючи таблицю розчинності, вкажіть розчинну
речовину:
А. NaCl ; Б. PbCl2
; B. AgCl, Г. Ca(OH)2.
4. Розчин, в якому певна речовина за даних умов ще може
розчинитися,називається:
А.Насичений; Б. Ненасичений; В. Концентрований; В. Розведений.
5. Щоб ненасичений розчин солі перетворити в насичений,
потрібно:
А. Додати води;
Б. Додати солі; В. Нагріти; Г. Охолодити.
6. У розчині масою 80 г . знаходиться 10 г . харчової соди NaHCO3. Визначте масу води у розчині.
А.90г.; Б. 70г.; В. 8г.
Д. 800г.
7. Як змінюється розчинність більшості твердих речовин з
підвищенням температури?
А.
Спадає; Б. Зростає; В. Не змінюється.
8. Розчин, у певному об’ємі якого міститься мало розчиненої речовини, називається:
А.Насичений; Б. Ненасичений; В. Концентрований; Г. Розведений.
9. Встановити відповідність між даними дисперсними
системами та їх класифікацією:
1.Суспензія А.Розчин білка у воді.
2. Емульсія Б.Суміш бензину з водою.
3. Істинний
розчин В. Суміш глини з водою.
4. Колоїдний
розчин Г.Розчин цукру у воді.
10. Знайдіть формулу кристалогідрату, назва якого «мідний
купорос»:
А.
Na2SO4·10 Н2О;
Б. CaSO4·2H2 О; В.CuSO4·5H2O; Г. Na2СO3·10Н2О.
Варіант ІІ
1.Виберіть, у яких випадках утворяться істинні розчини,
якщо речовини добре перемішати у воді:
А. Пісок Б Оцтова кислота; В.
Бензин; Г. Кухонна сіль.
2. Розчин-це:
А.Неоднорідна система з кількох
компонентів.
Б.Однорідна
система сталого складу, що складається з кількох компонентів.
В.Однорідна
система змінного складу, що складається
з кількох компонентів.
3. Використовуючи
таблицю розчинності, вкажіть розчинну речовину:
А. NaNO3
; Б. BaSO4; B.
CaCO3 Г. CaSO4.
4. Розчин, в якому певна речовина за даних умов вже
більше не може розчинитися,називається:
А.Насичений; Б. Ненасичений; В. Концентрований; В. Розведений.
5. Щоб насичений розчин солі перетворити в ненасичений, потрібно:
А.
Додати води; Б. Додати
солі; В. Нагріти; Г. Охолодити.
6 До 20г цукру
додали 100г. води.Визначте масу утвореного розчину.
А.80г.; Б.120г.; В.50г.; Г.2000г.
7. Як змінюється
розчинність газоподібних речовин з підвищенням температури?
А.
Спадає; Б. Зростає; В. Не змінюється.
8. Розчин, у певному об’ємі якого міститься багато розчиненої речовини, називається: А.Насичений; Б. Ненасичений; В. Концентрований; В. Розведений.
9. Встановити відповідність між даними дисперсними
системами та їх класифікацією:
1.Суспензія А. Холодець
2. Емульсія Б.Суміш олії з водою.
3. Істинний
розчин В. Суміш вапна з водою.
4. Колоїдний
розчин Г.Розчин кухонної солі у
воді.
10. Знайдіть формулу кристалогідрату, назва якого «
глауберова сіль»:
А. Na2SO4·10 Н2О;
Б. CaSO4·2H2 О; В.CuSO4·5H2O; Г.Na2СO3·10Н2О.
Відповіді:
І варіант
|
ІІ варіант
|
1.
Б, Г
|
1.
Б,Г
|
2.
Б
|
2.
В
|
3.
А
|
3.
А
|
4.
Б
|
4.
А
|
5.
Б, Г
|
5.
А,В
|
6.
Б
|
6.
Б
|
7.
Б
|
7.
А
|
8. Г
|
8. В
|
9. 1-В,
2-Б, 3-Г, 4-А
|
9. 1-В,
2-Б, 3-Г, 4-А
|
10. В
|
10. А
|
ІІ. Мотивація навчальної діяльності
Поняття «насичений»,
«ненасичений», «концентрований», «розведений» є досить широкими. Розчин
– це однорідна система змінного складу. Тобто кількість розчиненої речовини
може значно змінюватися.
Працюючи з розчинами важливо знати їхній склад, тобто
скільки розчиненої речовини міститься в розчині. В кулінарниг книгах, в
рецептах консервації вказують: 7% розчин солі. (щоб було смачно, треба взяти
солі не більше і не менше).
На пляшці з оцетом пишуть 9%, а есенції – 98%. Якщо ви
переплутаєте ці розчини, то страву не
можна буде їсти.
У аптеках готують 5% спиртовий розчин йоду.
Кількісний склад розчину виражають концентрацією
розчиненої речовини.
Концентрація
розчиненої речовини – це фізична величина, яка визначає кількісний склад
розчину.
Концентрація виражається
різними способами (масова частк, об’ємна, мольна, еквівалентна,
моляльначастка). Ми розглянемо одну з них – масову частку, навчимося визначати
масову частку, виготовляти розчини із заданою масовою часткою.
ІІІ. Вивчення нового матеріалу.
Масова частка розчиненої речовини – це
фізична величина, що дорівнює відношенню маси розчиненої речовини до маси
розчину.
mx
mроз.
mx – маса речовини Х
mx = ωх ∙ mроз.
mроз – маса розчину
mx
ωх
mроз. = m(Н2О) + mx
mроз
Vроз
ρ (Н2О) = 1 г/мл
Вимірюється масова частка в частках одиниці або %
Розглянемо малюнок
34
ω(NaCl) = 5% це означає, що в 100 г розчину знаходиться 5 г солі та 95 г води.
ω(NaCl) = 20% це означає, що в 100 г розчину знаходиться 20 г солі та 80 г води.
(Інтерактивна технологія «мозковий
штурм», на дошці в центрі пишемо пускове слово «розчини», а навколо записуємо
ідеї учнів.)
Назвіть приклади відомих вам
розчинів та зазначте їх фізичні властивості (колір, смак, прозорість).
Передбачувані відповіді:
Групуємо висунуті ідеї:
Прозорі розчини → безбарвні,
кольорові, солоні, солодкі, кислі.
Непрозорі розчини → каламутні.
Запитання:
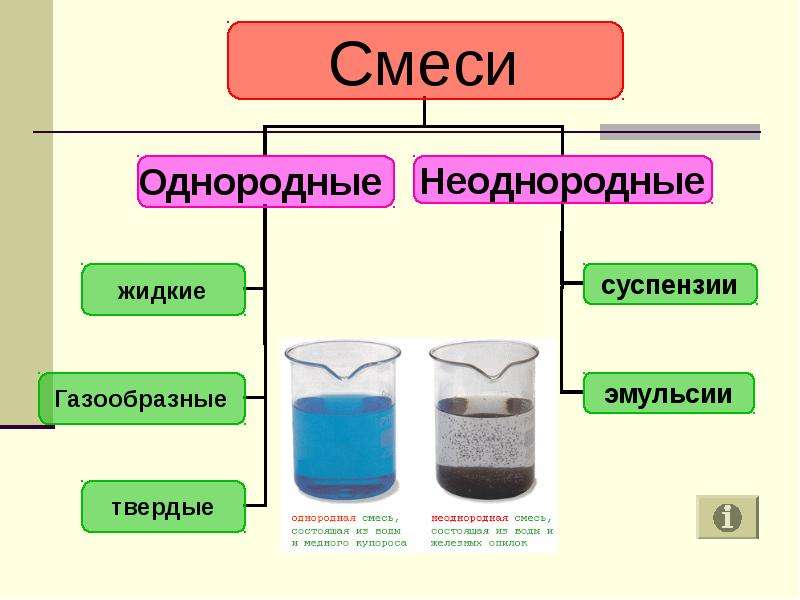
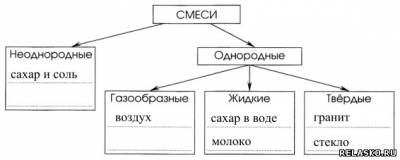
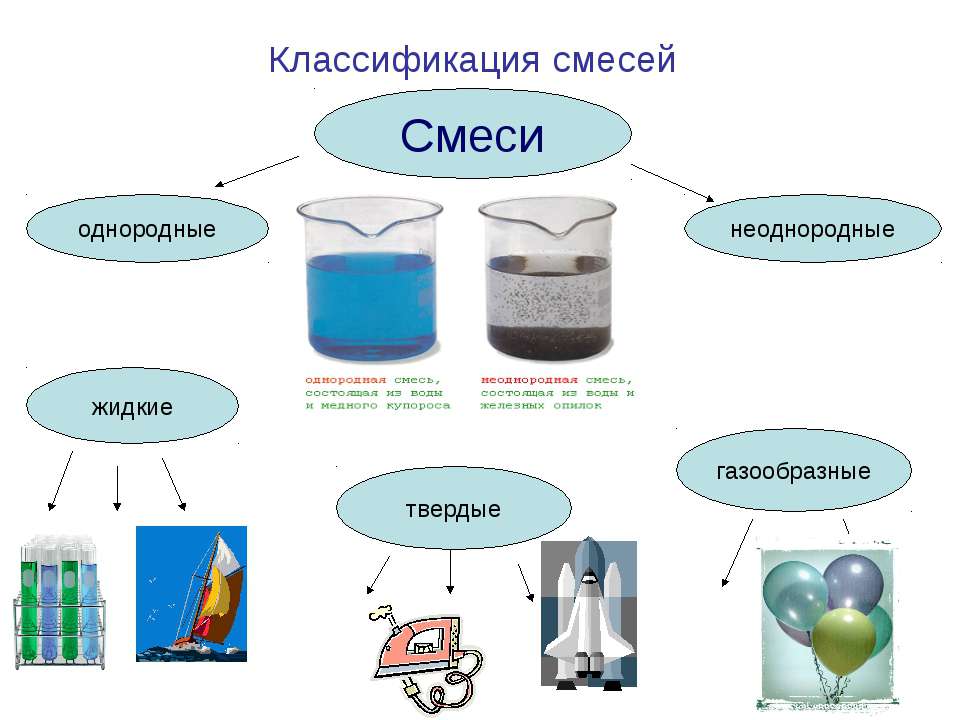
1. Як можна класифікувати прозорі й непрозорі розчини? (Однорідні і неоднорідні суміші.)
2. Чим відрізняються однорідні суміші від неоднорідних? (У
однорідних не видно частинок розчиненої речовини, а в неоднорідних видно.)
3. Що таке розчин? (Система, яка складається із
двох і більше компонентів та продуктів їх взаємодії.)
4. Поясніть, чим слід вважати розчини — механічними сумішами
чи хімічними сполуками?
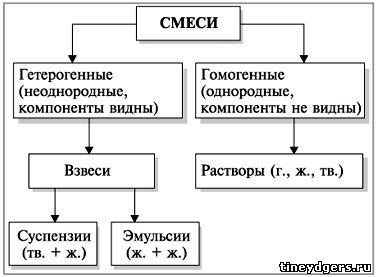
Серед розчинів можна виділити
однорідні й неоднорідні суміші.
Розчини, що є однорідними сумішами,
називаються істинними розчинами.
Розчини, що є неоднорідними
сумішами, називають
зависями (колоїдними
системами).
Запитання:
1. Які бувають зависі? (Робота з підручником.)
2. Що називається суспензією? Наведіть приклади. (Системи, що містять тверду та рідку
фази.)
3. Що називають емульсією? Наведіть приклади. (Рідина,
у якій містяться частинки іншої рідини.)
ІV. Розв’язування задач
1. В розчині масою 200 г міститься 5 г NaCl. Обчисліть
масову частку розчину.
mроз = 200
г mx
ω (NaCl) - ? 5
200
Відповідь: ω (NaCl) = 2,5%
2. У 100 г води
розчинили 15,6 г
калій нітрату. Визначте масову частку солі у розчині.
m(Н2О)
= 100 г mx
ω
(КNО3) - ?
mроз. = 100 + 15,6
= 115,6 г
15,6
115,6
Відповідь: ω (КNО3) = 13,5%
3. Приготувати розчин масою 50 г із масовою часткою
кухонної солі 5%.
m(роз.)
= 50 г m (NaCl)
= mроз∙ ω (NaCl)
ω
(NaCl) = 5% m (NaCl) = 50 ∙0,05 = 2,5
г
m (NaCl) - ? m(Н2О) . = mроз -
m(NaCl)
m(Н2О) - ?
V(Н2О) - ? m(Н2О) .
= 50 – 2,5 = 47,5 г
m(Н2О)
ρ (Н2О)
47,5
1
ІV.
Узагальнення і систематизація знань
На дошці вчитель складає
опорний конспект, який учні записують у зошити.




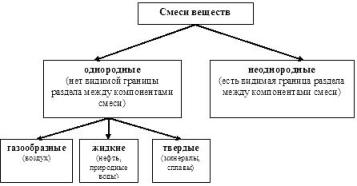
Запитання:
1. Що таке розчин?
2. Чим розчини відрізняються від механічних сумішей?
3. Як класифікують розчини?
5. Назвіть характерну ознаку істинних розчинів.
6. Чим відрізняються істинні розчини від зависей?
7. Які зависі вам відомі?
8. Що таке суспензії? Наведіть приклади.
9. Що таке емульсії? Наведіть приклади.
10. Яке значення розчинів у житті та практичній діяльності
людини?
V. Підсумок
уроку.
VI. Домашнє
завдання
Вивчити відповідний параграф підручника. Підготувати цікаві
повідомлення про розчини використовуючи мережу Інтернет.
ВИДЕО.
ПРАВИЛА ПРИГОТОВЛЕНИЯ СТАНДАРТНОГО РАСТВОРА.
ПРАВИЛА ПРИГОТОВЛЕНИЯ СТАНДАРТНОГО РАСТВОРА.
Комментариев нет:
Отправить комментарий